冷冻电磁机:以近原子分辨率可视化生物分子
2026-02-21Cryo-EM:以近原子分辨率可视化生物分子正在重塑结构生物学,因为它帮助研究人员在更接近现实生活的条件下观察蛋白质、复合物和病毒——无需使用晶体或过度激进的样本处理。Longlight Technology 支持冷冻电子显微镜项目,提供清晰的工作流程、透明的交付物和实用指导,帮助团队更快、更少死胡同地从“有前景的样本”迈向“可辩护的结构”。
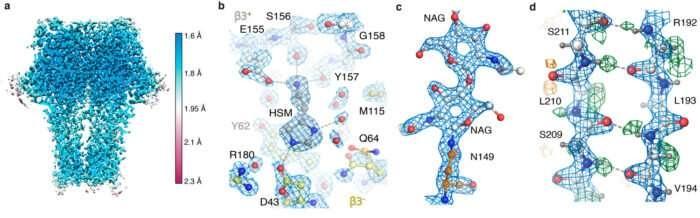
科学家们打破分辨率纪录,用单粒子低温电子显微镜可视化单个原子
我们不把冷冻电子显影(cryo-em)当作一种神秘的高端服务,只适用于完美样本,而是把它当作一个结构化的决策系统来对待:筛选现有样本,了解其功能,只有当样本真正准备好时才扩展到高分辨率数据收集。这种心态节省了时间、预算和宝贵材料——尤其是对于需要能够经受内部评审和同行评审结果的首次用户来说。
为什么低温电磁对现代结构生物学如此重要
什么是冷冻电磁
冷冻电子显微镜(Cryo-EM) 是一种通过将生物分子快速冷冻在一层薄玻璃状(类似玻璃)的冰层中,用电子显微镜成像它们来“观察”它们的方法。冷冻将分子锁定在近乎本体状态,无需化学固定或结晶,计算机结合多种二维视图来重建三维结构——对于表现良好的样品,通常能以近原子分辨率实现。
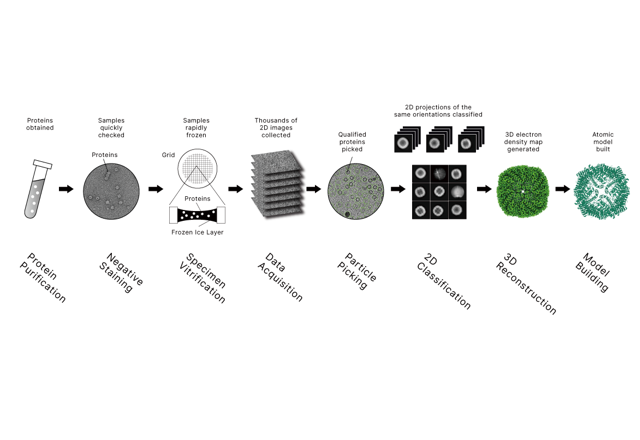
冷冻电磁工作原理(简视图)
•在溶液中制备样品(蛋白质、复合物、病毒等)
•通过快速冷冻使其变得玻璃状(无冰晶)
• 使用透射电子显微镜成像数千到数百万个粒子
•计算:对齐、分类和重建三维地图;有时会构建原子模型
主要冷冻电子显微镜方法
•单颗粒分析(SPA):最适合纯化蛋白质/复合物;这里常见最高分辨率。
•冷冻电子断层扫描(Cryo-ET):细胞或原生环境中结构的三维成像;非常适合空间上下文。
•微电子绕射(MicroED):针对晶体学较硬时的极小晶体(纳米/微晶)。
为什么人们选择冷冻电显
•无需种植晶体
• 捕捉分子接近其原生状态
•适用于大型复合体和许多“难度”目标
• 可揭示多种结构状态(运动/柔韧性)
在生命科学中,最快理解生物分子的方法通常是观察它的形状及其变化。冷冻电磁使得这些目标能够满足难度、柔韧或不稳定的目标——这正是许多团队最关心的目标。低温电子显微镜建立在透射电子显微镜基础上,能够根据样品行为和数据质量,重建从亚纳米到近原子分辨率的三维结构。
这在那些细节驱动决策的高影响力领域尤为重要:
• 药物发现:结合口袋、界面几何形状及诱导配合变化
• 抗体与疫苗:表位定位、中和机制及复杂稳定性
•病毒学:衣壳组织、构象转变及组装途径
•膜蛋白:通道、转运蛋白、受体和多通道复合物
许多现代靶不易结晶,有些甚至永远不会结晶。Cryo-EM通常会把“这太难结晶”转化为“现在可以测试”,因为工作流程是为迭代设计的:快速筛选,智能调整条件,然后在粒子表现正常后再放大。
低温电显机与X射线晶体学:初学者应了解
X射线晶体学依然是一种强大的方法,在合适的情况下可以达到极高的分辨率。但如果你是结构生物学项目规划的新手,关注风险和概率会有帮助,而不仅仅是理论上的最大分辨率。
冷冻电子显显电镜减少了几个常见的项目障碍:
• 无需结晶,消除了重大不确定性
• 近乎天然状态被玻璃化冰保存,提升生物学相关性
•灵活或动态目标可以被评估,而非“平均化”
• 硬靶点变得更加可行(膜蛋白、大型组装体、病毒)
•异质性有时可以通过计算方式被分离为不同的状态
•早期发现样品(视具体情况而定)可能实现较低的纯度容忍度
• 与重复结晶筛查相比,样品废弃物更少
简单来说:晶体学在晶体学中可以非常出色,但对于复杂目标、多组分复合物以及无法承受数月试错的项目,冷冻电磁显微镜往往是更可预测的路径。
Comparison of X-ray Crystallography, NMR and EM - Creative Biostructure
我们提供的结构解决方案:从筛选到近原子模型
在Longlight Technology,我们的冷冻电磁服务结构与真实项目的进展相匹配。我们将工作归为三个实用目标——以确保你的路径符合样本和你想要回答的问题。
样本适宜性评估与阴性染色筛查
在投资低温网格和高端显微镜时间之前,负染色筛查作为现实检验。通常在室温下进行,有助于回答第一个重要问题:样品是否表现得像结构样品?
负染色可以显示:
• 聚集或聚集
• 颗粒完整性与形态
• 尺寸分布与浓度适宜性
•粗糙异质性(同时出现过多“形状”)
• 不稳定或退化迹象
把负染色看作是质量门。它并非旨在发布高分辨率地图。它的目的是避免对尚未准备好的样本进行昂贵的数据收集——并以证据而非猜测为下一步优化指导。
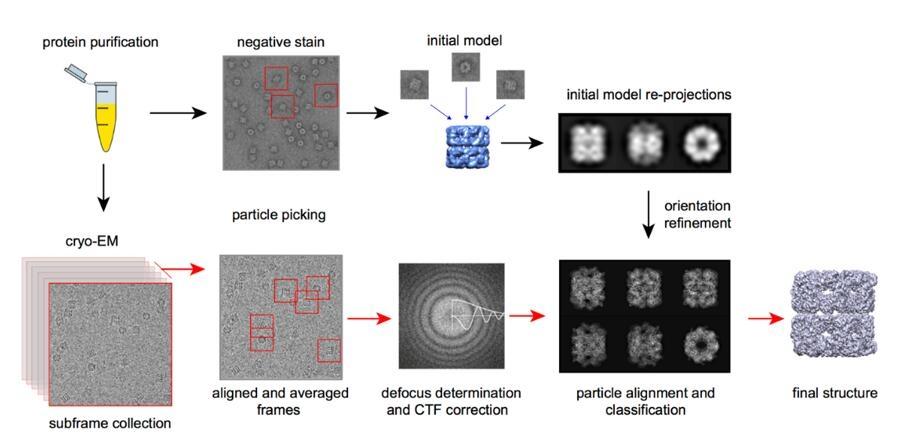
单粒分析实现高分辨率结构判定
对于许多可溶性蛋白质和复合物,单颗粒分析(SPA)是获得高分辨率结果的最常见途径。大型数据集包含来自多种方向的单个粒子视图。计算处理对准和分类这些粒子图像,并重建三维密度图。当地图支持时,可以构建和完善原子模型,揭示仅靠生化读数看不到的机制。
SPA是Cryo-EM:以近原子分辨率可视化生物分子的直接实践平台:结合界面、结构域运动以及活性、抑制或特异性的结构解释都可以自信地描述。
利用冷冻电子断层扫描进行原位结构分析
如果你的问题不是“这种纯化粒子长什么样”,而是“它在情境中是如何组织的”,那么冷冻电子断层扫描(Cryo-ET)更适合。断层扫描可以在更原生的环境中可视化结构,这对以下用途非常有用:
•膜相关组件
•大型细胞复合物
• 病毒-宿主交互组织
• 空间布局与建筑问题
当空间故事和分子形状同等重要时,通常选择冷冻外星。
我们的服务流程及您所获得的服务
冷冻电磁项目不应该让人觉得像个黑匣子。我们在每个阶段都构建了清晰的流程,让你始终知道发生了什么,观察到了什么,以及正在做出哪些决策。
典型工作流程:
项目咨询→NDA签署→服务协议确认、样品接收确认→质量检查→→阴性染色筛查→低温电子显电镜数据收集→数据处理→报告交付
交付物是为实际研究用途而设计的,而不仅仅是为了“漂亮的图片”。根据范围不同,您可以获得:
• 原始冷冻电子显磁胶片(如适用附有增益参考文件)
•关键中间处理输出
• 最终的3D密度地图,包含分辨率和质量指标
• 原子坐标模型(当密度支持模型构建时)
• 验证和交叉核查报告(例如结构质量评估)
• 通过安全的云或便携存储实现有组织的数据传输
目标很简单:你应该能够复制作品,必要时重新处理,并自信地发表——不必事后追逐文件,也不必怀疑结论是如何得出的。
匹配不同项目阶段的设备平台
不同的采样需要不同的乐器力量和策略。花钱买旗舰系统来回答一个基础筛选问题效率低下,而且常常拖慢项目进度。
我们的低温电磁服务能力由涵盖筛查的平台支持,包括高分辨率结构判定,例如:
• Talos L120C G2:高效的透视镜/冷冻电子显微镜筛查与评估
•Glacios 2(200 kV):适用于常规SPA和低温环境处理流程的强大主力系统
• Titan Krios G4(300 kV):旗舰平台,设计注重稳定性、自动化、吞吐量和顶级分辨率潜力
这种分层方法支持一个实用原则:在正确的时间使用正确的显微镜。筛选保持高效,只有当样本准备好进行高分辨率采集时才会进行。
实际项目需求、交付时间窗口及明确的下一步
如果你正在规划第一个结构项目,样品准备细节非常重要。大多数延迟并非由“显微镜”引起,而是由于样品不稳定性、聚集或缓冲元件不兼容等可避免的问题。
典型的最小样本指导:
•负染色:~1克/升,~100微升
•SPA(可溶性蛋白):~1 g/L,~100 μL
•SPA(膜蛋白):~1 g/L,~100 μL(通常可通过讨论调节)
典型缓冲器指导:
•pH 6.0–8.5
•盐浓度<200 mM
• 偏好低甘油和低叠氮化物(可逐案优化)
典型的交付窗口:
• 阴性染色筛查:1–2周
• SPA初步结局:6–8周
•SPA高分辨率模型(可实现时):~2–3个月
CTA:如果你想快速降低新目标的风险,可以先从阴性染色筛查开始。将您的样品详情(目标类型、缓冲液、浓度和估计纯度)发送给Longlight Technology,我们将根据您的科学目标和时间线推荐最高效的方法——负染色、SPA或低温ET。
最后,许多冷冻电子显微镜研究与上游和下游生物学相关联。Longlight Technology 还支持更广泛的分子生物学和基因组学工作流程,包括与 NGS 相关的仪器(如聚焦超声)以及常用消耗品和试剂盒(预制琼脂糖凝胶、核酸提取试剂盒和文库制备试剂盒),使您的结构工作能够顺畅地与发现、验证和发表准备的研究设计相衔接。