蛋白质复合物的交联MS如何启示构象变化
2026-02-22Cross-Linking MS for Protein Complexes is one of the most practical ways to "freeze" real protein contacts in place and then read them out by mass spectrometry—so you can learn how a complex changes shape, not just what it looks like in one snapshot. At Longlight Technology, we see many teams start with a simple question: Is my protein complex static, or is it switching between conformations that matter for function? This article explains, in a beginner-friendly way, what chemical cross-linking coupled with mass spectrometry (often called CL-MS or XL-MS) can teach you about conformational change, and how to turn results into decisions you can act on.
通过化学交联结合质谱分析蛋白质复合物的进展
1)什么是交联型多发性硬化症?
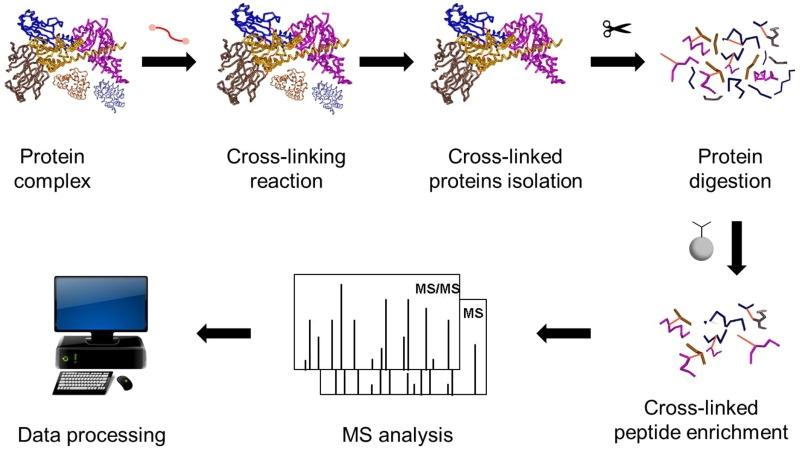
交联MS(通常写作XL-MS或CL-MS) is a method that helps you find which parts of proteins are close to each other—either within one protein or between proteins in a complex—by chemically "linking" them and then identifying those links by mass spectrometry.
简单来说,这个想法如下:
• Add a cross-linker (a small chemical "bridge")
它与特定氨基酸反应,并能共价连接两个彼此距离有限的残基。
• 将蛋白质消化成肽
酶(通常是胰蛋白酶)将蛋白质切割成更小的块。
• 运行质谱
MS检测肽类,包括交联肽对。
• 分析交联
每个识别的交联都变成一个距离约束:
"Residue A and residue B were close enough to be linked under these conditions."
它的用途
• 蛋白质-蛋白质相互作用(PPI)定位:复合体中谁接触谁
• 界面识别:哪些区域构成接触面
• 构象变化:比较条件(APO与配体结合、突变体与WT)以观察接触的出现或消失
• 支持结构建模:结合冷冻EM/X射线验证或完善模型
为什么它有价值
• Can capture weak or short-lived interactions (the covalent link "freezes" them)
• 通常不需要特殊标识
• 在比较多种条件时可以具有相对较高的通量
2)为什么构象变化如此困难 To 被俘
许多蛋白质复合物无法静止不动。它们会呼吸、旋转、开合和重新排列亚基,以响应配体、盐分、pH值、磷酸化或结合伴侣。传统的结构方法可以非常出色,但它们通常更倾向于稳定状态。如果一个综合体灵活、组装薄弱或寿命短暂,你可能只看到故事的一部分。
Cross-linking helps because it can covalently connect two residues that come within a certain distance. In plain language, it marks "these two positions were close enough to touch" at the time of reaction. Side-by-side cross-link comparisons—ligand-free vs bound, low vs high salt, wild-type vs mutant—tell you if the complex compacts, expands, or reconfigures.
✅ 给初学者的实用建议:体型变换是整体变换。XL-MS能超越最稳定构象,看到溶液中态谱。
交联质谱服务 |MtoZ生物实验室
交联多发性硬化症在实际中测量的哪些方法
多发质化酶的化学交联可以定量残基的邻近性和相互作用模式,是研究PPI的标准方法。交联剂与蛋白质上的官能基反应,可以连接两个或多个相互作用的蛋白质(或连接一个蛋白质中的两个位置)。交联后,质谱分析交联肽,从而描绘相互作用网络并识别作用位点。
这对构象变化意味着什么?
• 如果一组交联仅在配体结合后出现,则表明在结合态形成了新接触。
• 如果某些交叉链接消失,说明这些网站不再关闭——也许是复合体开放或域名迁移。
• 如果亚基之间的交联发生偏移,可能表明亚基重排或组装路径不同。
✅ 你从这种方法中获得什么(以及为什么它很重要):
• 无需特殊化学标签→保持蛋白质接近原生形态,减少实验负担。
• 捕捉短暂或弱相互作用→共价键可保留纯化或分析过程中断裂的接触。
• 高通量和快速分析速度→需要高效比较多种条件或构件时非常有用。
• 部分项目→可进行细胞内交联,这有助于你更贴近其原生细胞环境而非仅限体外研究复合物。
4)阅读 "运动" 来自交叉链图样
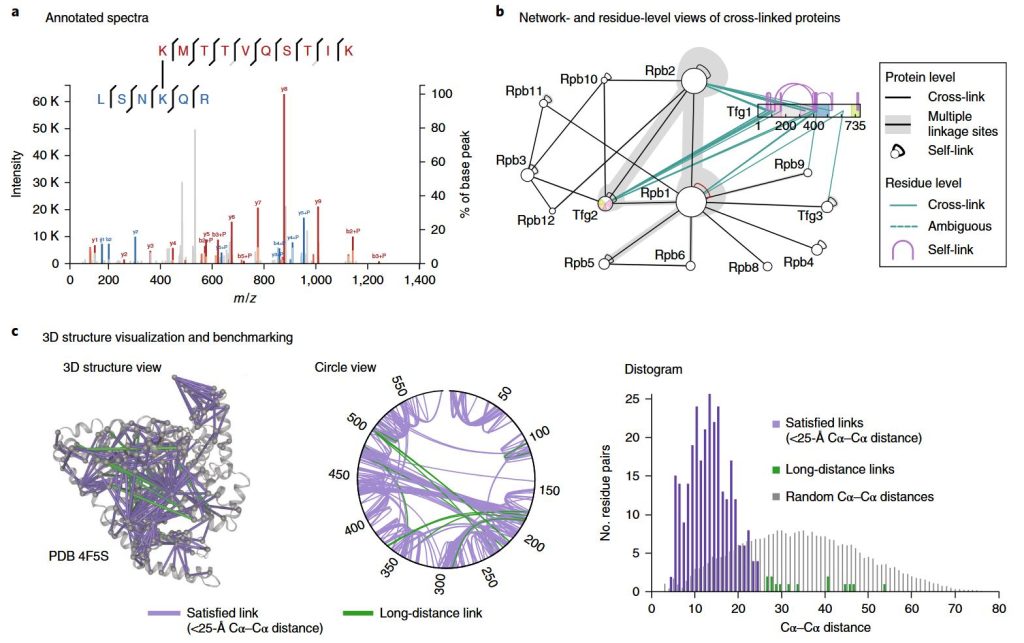
初学者有时会认为一个交叉链接就等于一个答案。实际上,价值来自于模式。
一个有用的思考方式是:交联是距离约束。当复合物构象发生变化时,两个残基之间的距离也随之改变。XL-MS不能总告诉你旋转的确切角度,但它能告诉你区域是否可能更靠近或更远,以及相互作用映射是否发生了变化。
以下是XL-MS常见的体型故事:
✅ 压实与开启
如果你在某一条件下看到更多跨越远处区域的蛋白内交联,蛋白质可能正在采取更紧致的状态。如果这些环节消失而其他环节上升,那它可能正在打开。
✅ 接口切换
如果亚基A和B之间的交联变弱,而A和C之间的连接增强,则提示加权组件或接口开关。
✅ 配体或突变稳定
A ligand that "locks" a conformation often increases the reproducibility of a specific cross-link set and reduces mixed patterns.
从实际角度看,这可以指导下一步:制造哪个突变体,截断哪个域,哪个缓冲条件稳定复合体,或用其他方法验证哪个接口。
5)XL-MS与冷冻电显或X射线结合时,结果更强
XL-MS常与低温电子显微镜(cryo-EM)和X射线晶体衍射配合使用,用于生物结构研究。当构象变化是核心问题时,这种组合尤其有用。
• 冷冻电磁可为主导态提供结构模型。
• XL-MS可以验证模型是否与溶液行为一致,并能标记冷冻电显可能采样不足的替代状态。
• X射线能够提供高分辨率的区域,而XL-MS则帮助将区域置入柔性组件中。
✅ 一个实用的流程:先用XL-MS来判断你的复合体是否异构。如果是这样,你可以设计出能丰富某一状态的条件,再大力投资高分辨率结构。
6)服务工作流程 一个长光技术
许多实验室希望获得蛋白质复合物交联MS的见解,但不想在内部建立完整的流程。Longlight Technology 通过清晰的服务流程支持经验丰富的团队和首次用户。
您可以发送交联样本,或联系我们制定交联计划并提交样本。我们完成完整的工作流程,包括酶消化、肽浓缩、质谱检测、数据分析以及实验报告的交付。这种端到端方法很重要,因为构象解释依赖于各步骤的一致处理。
✅ 这对你作为客户意味着什么:
• Fewer handoff errors between steps, and fewer "unknowns" when you compare conditions
• 一份以可作解释为组织的报告,而不仅仅是原始识别
• 当你需要测试多个构造或处理条件时,迭代速度更快
如果您的项目涵盖基因组学或上游检测开发,Longlight还提供前沿的基因组学解决方案、先进的实验室仪器以及高品质试剂和耗材,旨在提升现代实验室的效率和准确性——支持从分子生物学到精密分析的研究流程。
7)实用CTA:将构象问题转化为可检验的证据
体型变化不是附带细节。它通常决定靶点是否可下药,复合物是否能正确组装,以及突变是否真正具有破坏性。蛋白质复合物的交联多发性硬化症为你提供了可以比较不同疾病的证据,帮助你停止猜测,开始设计。
✅ If you are planning a conformational-change study, consider starting with one "comparison set":
• Apo与配体结合(或抑制剂结合)
• 野生型与单一接口突变体
• 一个稳定缓冲器与一个应力缓冲器(盐/pH范围)
号召性: 如果您想制定一个清晰、适合初学者的XL-MS计划,针对您的蛋白质复合物,请联系Longlight Technology,讨论您的目标(相互作用映射、界面验证或构象比较)。我们可以帮助您选择切实可行的交联策略,并提供支持您下一次实验或下一个结构模型的可解读报告。