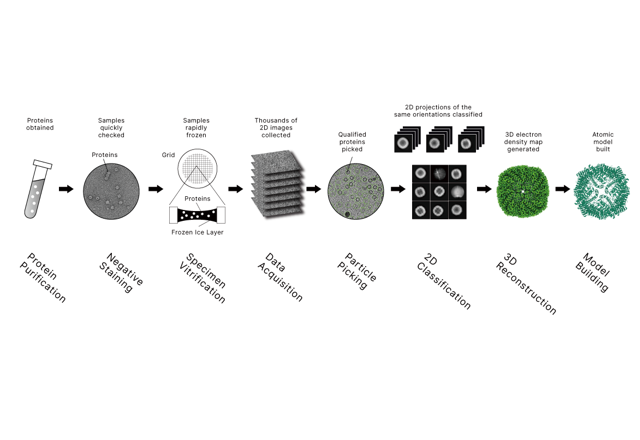
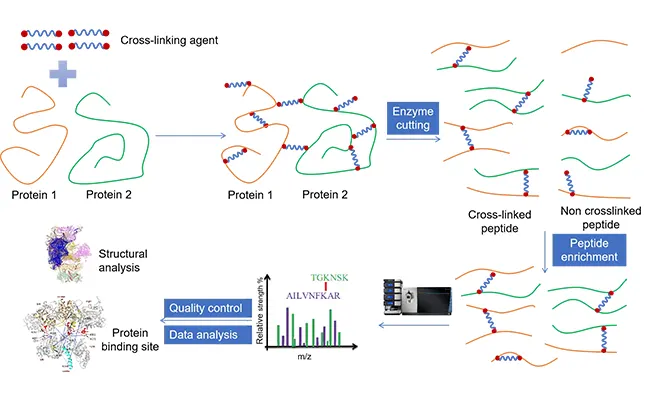
ChIP-seq 故障排除入门:逐步修复低信号
2026-02-28ChIP-Seq故障排查通常从一个简单的症状开始——信号不足——但真正的原因通常分布在染色质质量、抗体表现、免疫沉淀条件和文库质量控制等方面。在Longlight Technology,我们支持运行ChIP-Seq检测组蛋白标记和转录因子的实验室,我们发现不同仪器和样本类型中重复出现相同的“安静失效点”。这份ChIP-Seq故障排除101指南,一步步引导初学者按逻辑顺序恢复信号,使用可在一次运行中验证的实用检查点。
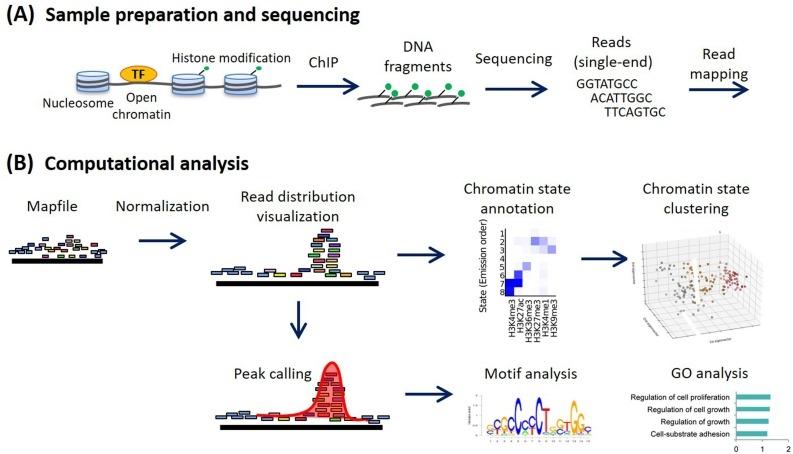
ChIP-seq 分析方法:实用工作流程与高级应用 - ScienceDirect
1)定义 "信号低" 在你改变任何东西之前
信号低可能意味着不同情况:峰太少、已知位点富集薄弱,或者库看起来正常但映射不好。 良好的ChIP-Seq故障排除 首先明确标注失效模式,因为每种模式指向不同的修复方法。
一个适合初学者定义问题的方法是检查三层:
✓ 生物学层:目标是否存在于你的细胞状态(刺激与静息状态、分化阶段、治疗时机)?
✓ 富集层:ChIP DNA在阳性对照位点与阴性位点上,是通过qPCR富集吗?
✓ 测序层:你有足够的唯一映射读段和合理的重复层吗?
如果你无法回答这三点,就不要“优化一切”。先做一个受控实验:保持样本不变,测序深度适中,只改变一个疑似变量。
2)从染色质开始:片段大小 一个ND损失控制
当实验室询问为什么ChIP“无效”时,最常见的根本原因是染色质过度断裂、缺失,或在清理过程中丢失。在ChIP-Seq故障排查中,染色质是你的基础——如果它不一致,后续的每一步都会变成杂音。
对于基于声波的工作流程,许多实验室目标是采样150–300碱基对的片段,以实现尖叫尖叫和免疫沉淀的稳定。如果片段大多较大(例如>500碱基对),抗体难以高效拉取靶点复合物。如果片段太小,你可能会破坏表位或通过释放非特异性DNA来增加背景。
你可以立即完成的实用检查点:
• 在逆交联和清理后测量DNA(而不仅仅是IP之前)。这里大幅下降意味着珠子/柱子或恶劣环境的损失。
• 比较不同样本的碎片化剖面。如果一个样本“完美”,另一个样本被涂抹或放大,重点关注裂解和超声处理,而不是先看抗体。
• 从每批次中保留一份“输入DNA”分量。这是你对qPCR和文库QC的基础。
在Longlight Technology,我们建议将染色质制备视为受控的制造步骤:固定缓冲液成分,保持超声波检测时样品温度稳定,并记录精确的循环设置。微小的偏差会导致后期峰值强度的巨大差异。
3)抗体契合度:特异性、批次变异, 一个ND控制
如果染色质看起来合理,ChIP-Seq故障排查的下一步是抗体的选择和验证。信号低通常是由于使用一种“对西方病毒有效”但对ChiIP弱的抗体,或者是批次间的变异性所致。
良好的抗体策略围绕对照组建立:
✓ 阳性对照靶点:具有强健富集的组蛋白标记(常用以确认工作流程健康)。
✓ 阴性对照:用IgG或同型对照来估算背景拉下。
✓ 已知位点qPCR:目标有一个或两个已发表的阳性位点,加上一个基因沙漠区。
对于转录因子,信号本身可能低于组蛋白标记。这意味着你的抗体必须具有高亲和力,且你的IP条件必须干净。如果你是TF ChIP的新手,不要一开始就改变序列深度。首先通过qPCR确认富集效果。如果qPCR浓缩较弱,更多的读段通常会产生更多噪声。
实用提示:更换抗体批次时,如果可能的话,重新检查同一批染色质的浓集情况。如果批次更换导致信号中断,工作流不一定是“错误”的——你的试剂性能发生了变化,你的排查路径应该反映这一点。
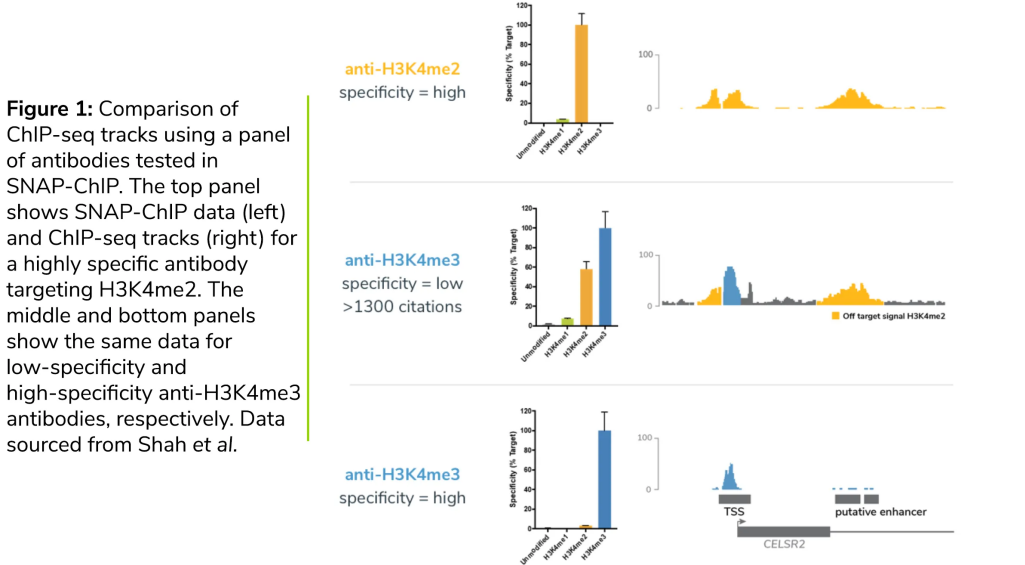
为您的实验选择合适的ChIP抗体——EpiCypher
4)干净的IP优化序列——无猜测
除了染色质和抗体,IP化学(珠子、洗净液、培养)是下一个热点。信号低通常是背景问题。
✓ 珠子选择:选择适合你抗体种类/同型的蛋白A/G。
✓ 抗体剂量:调整剂量以避免弱拉下或非特异性DNA升高。
✓ 洗涤平衡:校准严苛度以去除噪声,同时保留弱但真实的相互作用。
一个实用的新手规则是每次运行只调整一个轴:
• 如果存在峰值但较弱,则增加有效捕获(略多抗体,改善珠体结合,延长孵育时间)。
• 如果峰宽且噪声大,则提高特异性(更强的洗涤,更好的阻断,减少抗体过载)。
从制造商角度看,Longlight Technology设计免疫沉淀试剂和磁珠系统以最大限度减少处理过程中的损失,因为样品损失看起来就像“低信号”。顺畅的珠子分离、固定一致和干净的清洗步骤减少了操作员间的差异——这对培训新员工的团队尤其重要。
5)图书馆质量控制:何时 "良好的DNA。" 信号依然很低
有时ChIP的DNA富集是真实存在的,但最终数据仍然平淡无奇。在ChIP-Seq故障排查中,这通常指向库构建或测序指标。
常见的库级信号低导致原因:
✓ 过度扩增:过多的PCR循环会膨胀重复序列并减少可用的唯一读段。
✓ 适配器/引物伪影:这些伪影消耗测序读段,但不提升靶标覆盖率。
✓ 复杂度低:通常由极低的ChIP基因输入或清理过程中的损失引起。
在重新运行整个ChIP之前需要注意的事项:
• 文库大小分布(你希望有一个干净的峰值,而不是多个意外峰值)。
• 比对后重复率和唯一映射率。
• 峰值读数比例(FRiP)相对于你内部基线的趋势(即使是初学者也能追踪“更好与更差”的跑次)。
如果你怀疑文库过度循环,一个简单的改进是减少循环次数并提高上游捕获效率(更好的染色质恢复和IP特异性)。更深层次的测序无法弥补低复杂度的库。
6)步-作者-阶梯信号恢复,你可以明天开始
一个实用的序列,优于临时调整:
✓ 步骤1:确认染色质片段为~150–300碱基对,并确认逆交联后DNA恢复。
✓ 步骤2:在文库准备前通过qPCR检查一个阳性位点和一个阴性位点的浓缩。
✓ 步骤3:添加适当的控制(输入IgG),以区分“无富集”和“高背景”。
✓ 步骤4:一次调整一个变量(珠子、抗体量、洗涤硬度)的IP条件。
✓ 步骤5:在假设测序深度为问题之前,先审计库的指标(重复、映射、大小分布)。
CTA(Longlight Technology): 如果你想要更快的路径,请联系Longlight Technology,获取ChIP-Seq故障排查清单和逐样本诊断工作表(染色质→IP库→库)。我们还能推荐对照设计和试剂配对策略,以减少变异性,帮助初学者更早达到稳定浓缩。
信号低确实令人沮丧,但很少是神秘的。通过严格的ChIP-Seq故障排查流程——从染色质完整性、抗体匹配、IP特异性,最后到文库质量检测——你可以将一次弱测试转化为可重复的方案,并可跨样本、团队和项目扩展。